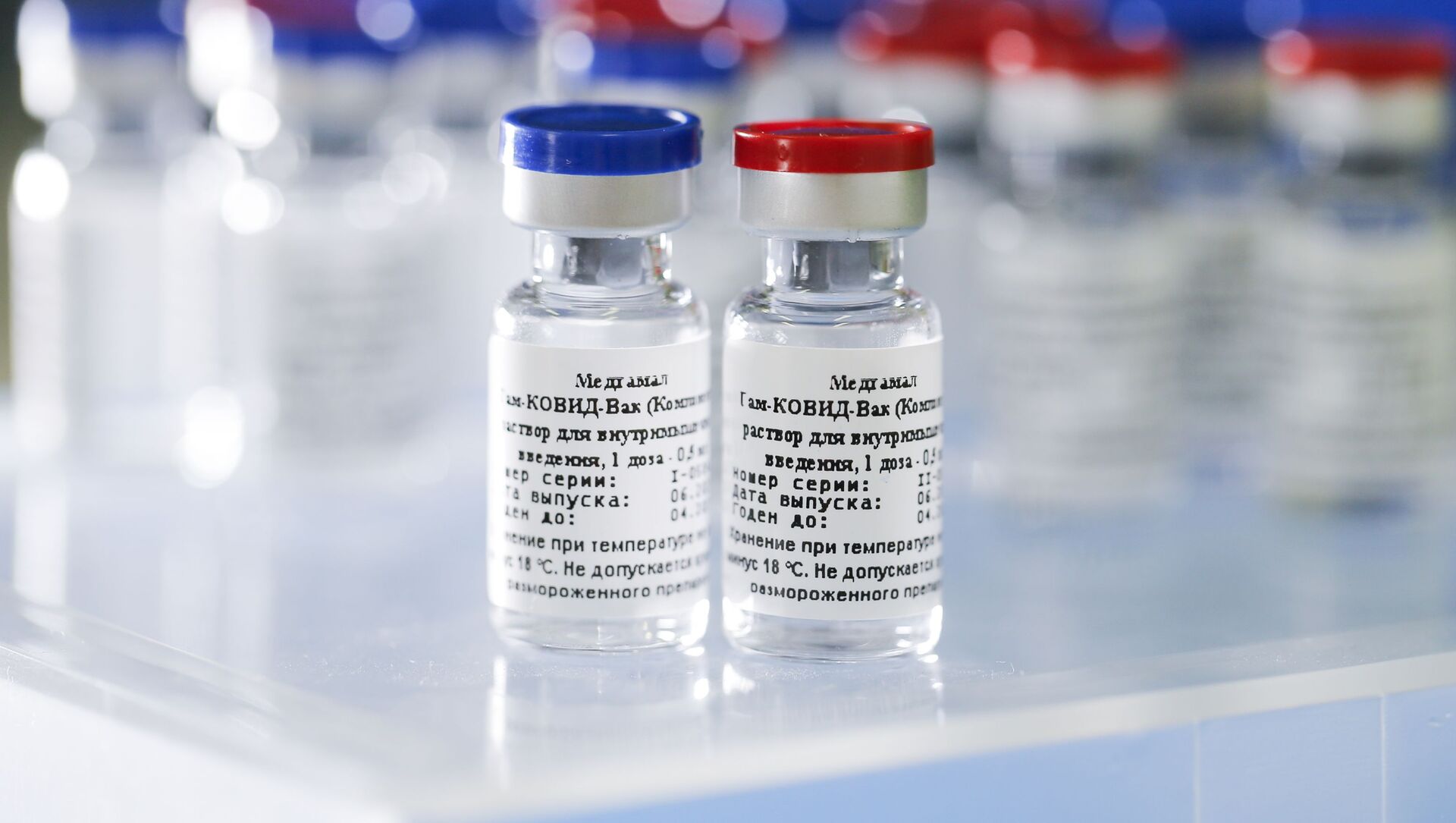
Autoritatea de reglementare a medicamentelor din Uniunea Europeană, Agenția Europeană a Medicamentului EMA, a finalizat etapa de consultare științifică a dezvoltatorului vaccinului rusesc împotriva coronavirusului „Sputnik V”; acum este posibil să fie depuse documentele pentru înregistrarea pe piața UE, a declarat agenția pentru RIA Novosti.
„La această etapă, putem spune că Centrul Național de Cercetare pentru Epidemiologie și Microbiologie Gamaleya a primit consultări științifice de la EMA cu privire la dezvoltarea vaccinului împotriva COVID-19 „Sputnik V” (cunoscut și sub numele de Gam-COVID-Vac) ... următorul pas, compania poate pregăti o cerere pentru o autorizație de introducere pe piață", a declarat sursa agenției.
El a explicat că "procesul de consultare științifică este un proces bine stabilit la EMA, care este disponibil tuturor companiilor pentru a facilita pregătirea programului lor de dezvoltare. EMA va consilia companiile pe baza celor mai recente sfaturi științifice".
Purtătorul de cuvânt al EMA a adăugat că agenția nu a primit încă o cerere de la dezvoltatorul vaccinului „Sputnik V”, momentul obținerii aprobării pentru piața UE de la EMA poate fi discutat după primirea unei astfel de cereri. „Deoarece nu am primit încă o cerere de înregistrare a vaccinului, nu putem indica un grafic convenit (de a primi o recomandare de la EMA - nota red.). De îndată ce vom primi o astfel de cerere de la companie, vom vom anunța despre acesta", a declarat reprezentantul autorității europene de reglementare a medicamentelor, răspunzând la o întrebare din partea RIA Novosti cu privire la posibila perioadă de timp pentru obținerea unui certificat de înregistrare.
În cazul eliberării unei autorizații condiționate de introducere pe piață și aprobarea de către Comisia Europeană, vaccinul rusesc poate fi furnizat centralizat către UE. Uniunea Europeană, chiar înainte de apariția primelor vaccinuri aprobate împotriva coronavirusului, a luat o decizie cu privire la achiziția centralizată a acestora. În total, au fost semnate contracte cu șase producători.
În prezent, pe piața UE sunt autorizate vaccinurile de la Pfizer / BioNTech (achiziționează până la 600 de milioane de doze), Moderna (160 de milioane de doze) și AstraZeneca (până la 400 de milioane de doze). În plus, CE a încheiat contracte pentru furnizarea de vaccinuri către UE cu Johnson & Johnson, Sanofi-GSK, CureVac. Până acum, acești dezvoltatori nu au solicitat încă autorizarea medicamentelor lor pe piața UE, dar în viitorul apropiat este așteptată o cerere de la J&J.
Astfel, datorită contractelor Comisiei Europene, țările UE vor putea avea acces la peste 2,3 miliarde de doze de vaccinuri anti-coronavirus. UE se așteaptă ca până la sfârșitul verii, aproximativ 70% dintre europeni să fie vaccinați.
Fii la curent cu toate știrile din Moldova și din lume! Abonează-te la canalul nostru din Telegram >>>
Privește Video și ascultă Radio Sputnik Moldova